M. hyo
Infezioni da Micoplasma hyopneumoniae
Mycoplasma hyopneumoniae (M. hyo) è il principale agente patogeno della polmonite enzootica (EP), malattia respiratoria cronica del suino e uno degli agenti principali coinvolti nel Complesso della Malattia Respiratoria dei Suini (PRDC) (Maes et al. 2017). EP è caratterizzata da tosse cronica, non produttiva, tasso di crescita e Indice di conversione alimentare ridotti (Sibila et al. 2009), in genere con mortalità bassa o nulla. PRDC si sviluppa come conseguenza di coinfezioni da agenti patogeni batterici e virali, in particolare il virus della Sindrome Respiratoria e Riproduttiva suina (PRRSV), il virus dell’Influenza suina (SIV) e il Circovirus suino tipo 2 (PCV2) (Sibila et al. 2009). PRDC può provocare un aumento della mortalità e gravi riduzione delle performances. La minaccia maggiore per l’economia dell’allevamento è rappresentata dalla riduzione dell’incremento ponderale giornaliero e dal possibile aumento del costo di medicazione. Spesso l’infezione da M. hyo sembra avere un decorso subclinico, in cui solo la crescita è ridotta.
Micoplasma hyopneumoniae
M.hyo è uno dei più piccoli microrganismi autoreplicanti privi di parete cellulare. Il patogeno non è in grado di sopravvivere a lungo al di fuori del suo ospite, ma negli aerosol la sua sopravvivenza aumenta poiché può rimanere infettivo fino a 31 giorni in acqua a 2-7 °C (Villareal 2010).
L’impatto clinico delle infezioni da M.hyo è determinato da diversi fattori, quali le condizioni ambientali, le pratiche di gestione, le co-infezioni e anche dai diversi livelli di virulenza tra gli isolati di M.hyo. La variabilità dei diversi isolati di M.hyo è stata descritta a livello antigenico, proteomico, trascrittomico, patogenico e genomico ed anche nella loro virulenza (Meyns 2007, Vicca 2003, Betlach 2019). Sebbene la patogenesi non sia stata ancora del tutto compresa, è stato riscontrato che contribuiscono alla virulenza del patogeno alcune proteine (principalmente le adesine), ma anche i geni coinvolti nel metabolismo e nella crescita.
Ceppi ad alta virulenza inducono segni di malattia più rapidi e più gravi rispetto ai ceppi a bassa virulenza (Villareal 2009). I ceppi a bassa virulenza inducono anche una sieroconversione più tardiva. Tuttavia, l’esposizione pregressa a un ceppo a bassa virulenza non riduce le lesioni dovute ad un’infezione successiva da ceppi M.hyo ad alta virulenza.
La co-infezione con più di un ceppo in un suino o in un gruppo di suini potrebbe causare lesioni polmonari più gravi (Michiels et al., 2017)
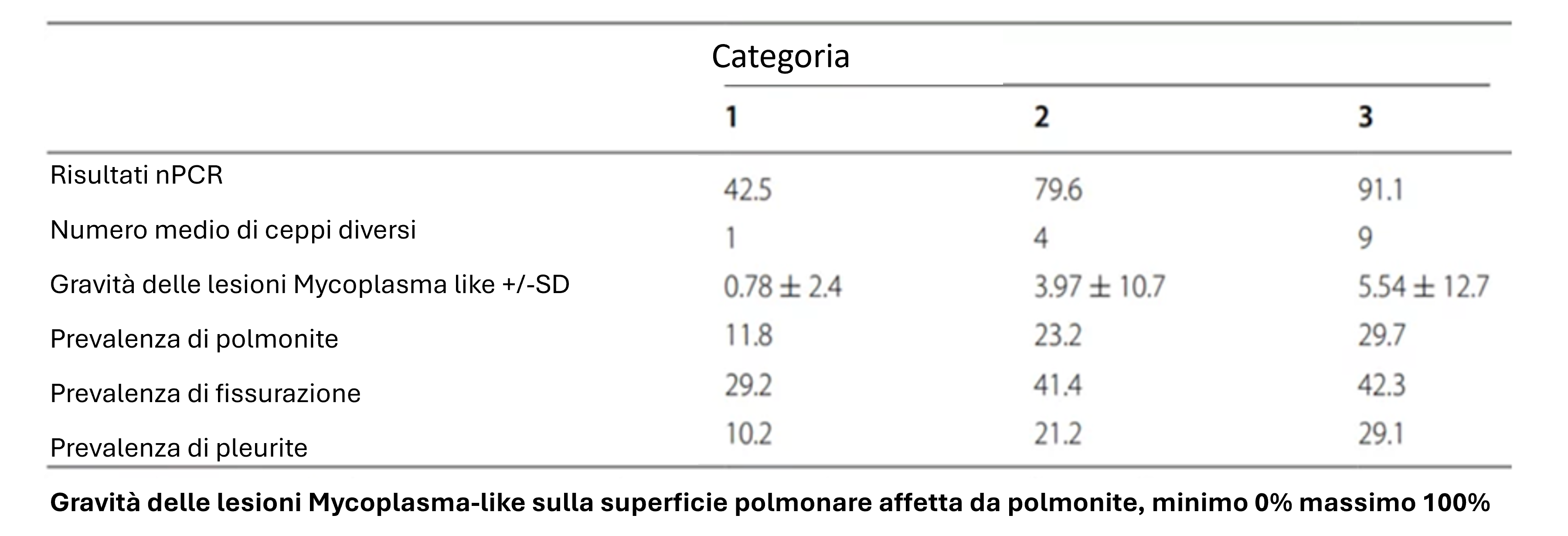
Prevalenza di risultati nPCR positivi, numero medio di ceppi diversi, gravità delle lesioni Mycoplasma-like +/-SD, prevalenza della polmonite, fissurazioni e pleurite espresse in percentuale. (Michiels et al., 2017)
1 = gruppi con un solo ceppo rilevato, 2 = gruppi con 2-6 ceppi diversi e 3 = gruppi con 7 ceppi
La Malattia
M.hyo è il principale agente patogeno della polmonite enzootica (EP), una malattia respiratoria cronica dei suini, e uno dei principali agenti coinvolti nel Complesso della Malattia Respiratoria dei Suini (PRDC). La polmonite indotta da M. hyo è considerata una delle malattie croniche più diffuse e importanti nei suini. La prevalenza nella popolazione mondiale suinicola è stimata raggiungere l’80% (Batista 2006). Quasi tutti i gruppi commerciali di suini negli Stati Uniti (oltre il 99%) sono affetti da polmonite da micoplasmi.
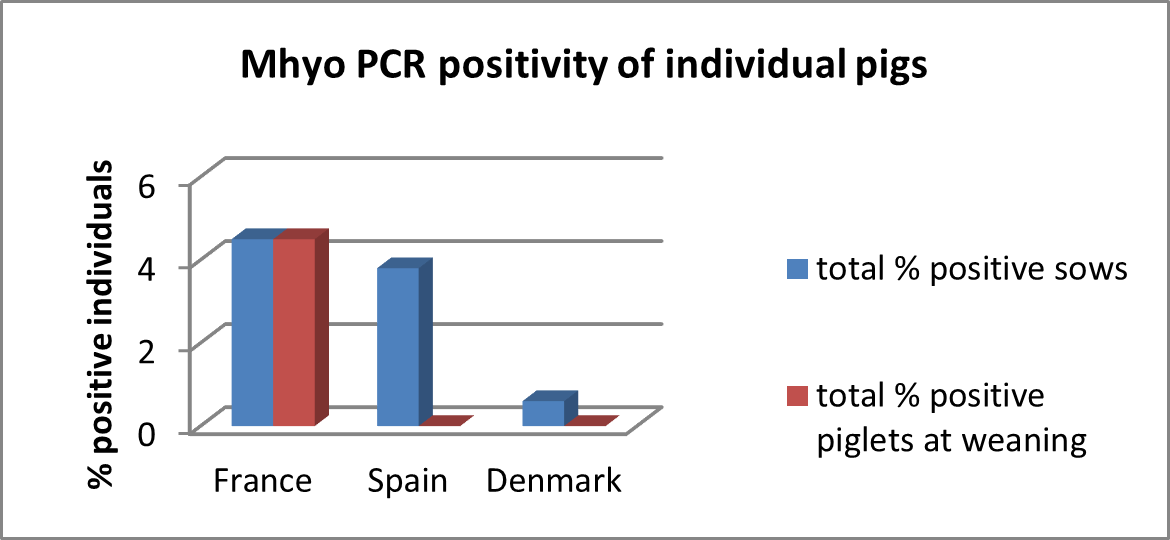
Le scrofe e i suinetti degli allevamenti da riproduzione sono considerati i serbatoi d’infezione da M.hyo per l’intero sistema produttivo. Si ritiene che la circolazione di M.hyo avvenga tra le scrofe presenti e sia trasmessa alle scrofette in arrivo, che sono in grado di mantenere l’agente patogeno all’interno dell’azienda e sono responsabili della maggior parte della diffusione batterica ai suinetti neonati. L’infezione da M. hyo ha lunga durata, fino a 240 giorni (Pieters 2009), complicando lo scenario già lento di trasmissione della malattia osservato nei gruppi di scrofe.
La positività è diversa nelle varie categorie di età. Tipicamente, la circolazione più importante si verifica nei suini in accrescimento. Nella maggior parte delle aziende convenzionali la prevalenza nei suini svezzati è molto bassa (Krejci 2019)
EP è caratterizzata da tosse cronica, non produttiva, ridotti velocità di crescita e indice di conversione alimentare (Sibila et al. 2009), in genere con mortalità bassa o nulla.
PRDC si sviluppa a causa di coinfezioni da agenti patogeni batterici e virali, in particolare Virus della Sindrome Respiratoria e Riproduttiva suina (PRRSV), virus dell’Influenza Suina (SIV) e Circovirus Suino tipo 2 (PCV2) (Sibila et al.2009). PRDC può provocare un aumento della mortalità e gravi cali nelle performances. La minaccia principale per l’economia dell’allevamento è rappresentata dalla diminuzione dell’incremento ponderale giornaliero e dall’eventuale aumento del costo di medicazione. L’infezione da M.hyo spesso sembra avere un decorso subclinico, dove solo la crescita è ridotta. La dinamica e la durata della tosse sono importanti per la stima dell’impatto di EP sul ritardo della crescita. È difficile valutare l’effetto economico della polmonite da micoplasma a causa dell’origine multifattoriale del PRDC. Si è registrata una diminuzione del 17% nell’aumento di peso giornaliero e una diminuzione del 14% nell’efficienza alimentare nei gruppi colpiti da polmonite enzootica (Straw 1989).
Quando i suini sani M. hyo-free sono mescolati a gruppi positivi a M. hyo e sono stati quindi esposti all’infezione naturale, le loro prestazioni sono diminuite. L’ IPG dei suini con una polmonite micoplasmica non complicata rispetto a quelli rimasti M.hyo-free si riduce di oltre 60 g al giorno dopo aver effettuato i necessari adeguamenti per gruppo, box, peso e sesso (Rautiainen et al. 2000).
La presenza dell’infezione è di solito confermata dalla sieroconversione specifica per M.hyo o dal rilevamento dei patogeni mediante PCR nei tamponi laringei (Pieters et al. 2017, Sibila et al. 2009). Il tessuto polmonare infettato con M.hyo aumenta la sua consistenza e mostra broncopolmonite catarrale con regioni di aspetto carnoso di colore da porpora a grigio. L’aumento di consistenza può essere osservato da 3-12 settimane dopo l’infezione. Le lesioni sono localizzate principalmente nei lobi apicali e cardiaci, nonché nella parte anteriore dei lobi diaframmatici e nel lobo intermedio. Queste lesioni si risolvono dopo 12-14 settimane con formazione di fissure interlobulari (Maes et al. 2008). Considerando la cronicità di tali lesioni, la broncopolmonite con consolidamento cranio-ventrali dei polmoni è molto indicativa di EP anche nei suini al macello.
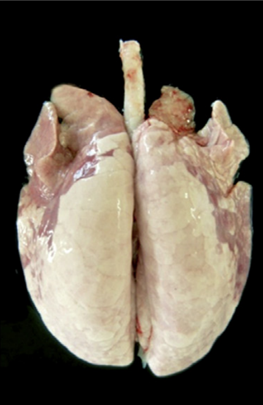
Esempio di polmone con lesioni derivate da infezione sperimentale M.hyo (Garcıa-Morante, 2016).